

Vol. 38 (Nº 32) Año 2017. Pág. 26
PALHETA, Lenilson F. 1; SANTOS FILHO, Benedito. G . 2; SIMÕES, Pedro H. O. 3; NOGUEIRA, Glauco A. 4; OLIVEIRA NETO, Cândido F. 5; SOUSA, Pablo R. F. 6
Recibido: 10/02/2017 • Aprobado: 23/03/2017
RESUMO: O trabalho teve como objetivo investigar as respostas de crescimento e as respostas ecofisiológicas de plantas jovens de castanheira-do-brasil sob deficiência hídrica. O delineamento experimental utilizado foi inteiramente casualizado com dois tratamentos: plantas irrigadas e não irrigadas, por três períodos (0, 5 e 9 dias). A condição de estresse hídrico afetou contrariamente o crescimento e os indicadores de trocas gasosas. Portanto, a falta de água por um período reduzido exerceu influência imediata no crescimento e desenvolvimento das plantas de castanheira-do-brasil. |
ABSTRACT: The objective of this work was to investigate the growth responses and the ecophysiological responses of young Brazil nut plants under water deficiency. The experimental design was completely randomized with two treatments: irrigated and non-irrigated, for three periods (0, 5 and 9 days). The condition of water stress adversely affected growth and indicators of gas exchange. Therefore, the shortage of water for a limited period had an immediate influence on the growth and development of young Brazil nut plants. |
A Bertholletia excelsa Bonpl. Conhecida como castanheira-do-brasil é uma das mais importantes espécies de exploração extrativista da Amazônia, com significativa participação na geração de renda das diversas comunidades amazônica (TONINI, 2011; AZEVEDO, 2014). Considerada árvore de grande porte, esta pode atingir 50 metros de altura (HAUGAASEN et al., 2010), tendo um fruto lenhoso, globular, extremamente duro, com tamanho variável e peso que obtém o nome ouriço e tem sementes ricas em gordura e proteínas de boa qualidade.
Estudos têm demonstrado ser uma das espécies com grande potencial para ser utilizado em programas de reflorestamento na região amazônica, devido ao seu bom desempenho de crescimento sob várias condições ambientais e as excelentes características silviculturais, como uma alta taxa de sobrevivência, baixa porcentagem de árvores bifurcadas, com caules longos e retos (COSTA et al., 2009, SCOLES et al., 2011).
O estabelecimento de plantios florestais, seja para fins comerciais ou restauração, depende de uma série de fatores, sendo a qualidade das mudas fundamental para o sucesso inicial (GASPARIN et al., 2014), sendo a água recurso essencial para o desenvolvimento da planta, uma vez que participa em todos os seus processos metabólicos, e sua ausência afeta muitos processos fisiológicos, como diminuição da atividade fotossintética juntamente com diminuição do volume celular (NOGUEIRA et al., 2001).
Mudas de castanheira-do-brasil em plantações jovens tem mostrado tolerância significativa à seca, exigindo um período de até 58 dias de irrigação de retenção para minimizar as taxas de câmbio de gás, indicando uma alta plasticidade fisiológica das espécies no campo (GOMES, 2012, FERREIRA et al., 2012). Entretanto, sob condições de casa de vegetação, pouco se sabe com relação ao seu comportamento quando submetidas à deficiência hídrica.
Diante do exposto objetivou-se investigar as respostas de crescimento e respostas ecofisiológicas de plantas jovens de castanheira-do-brasil sob deficiência hídrica.
O experimento foi realizado em casa de vegetação com cobertura plástica de 70% de luz solar, pertencente ao Instituto de Ciências Agrarias (ICA) da Universidade Federal Rural da Amazônia (UFRA), situada no município de Belém, Pará.
Foram selecionadas plantas jovens de castanheira-do-brasil, que apresentavam uniformidade de tamanho (aproximadamente 100 cm de altura), e transplantadas para vasos de plástico (30cm de altura x 25cm de diâmetro) com capacidade para 10 kg, contendo substrato de solo do tipo latossolo.
Durante 45 dias as plantas foram aclimatadas sendo irrigadas, diariamente, até a capacidade de campo. Após esse período, as plantas foram subdivididas em dois grupos: plantas irrigadas (tratamento controle) e não irrigadas (tratamento de déficit hídrico). Os indivíduos do tratamento controle, receberam irrigação diariamente, no período de as 8 e 16h, durante todo o experimento (9 dias) e as plantas do tratamento com déficit hídrico tiveram sua irrigação completamente suspensa por mesmo espaço de tempo.
As medições de trocas gasosas, crescimento e biomassa foram realizadas durante os dias de experimento (0, 5 e 9 dias) sendo utilizado o método destrutivo para as coletas de biomassa.
Para as trocas gasosas utilizou-se um analisador de gás infravermelho (IRGA Infrared Gas Analizer), modelo Li-6400 (Li-Cor, Biosciences Inc., Nebraska, EUA) onde foram realizadas medições pontuais de trocas gasosas no período de 9 e 11 horas que foi pré-determinado pela curva fotossintética, sendo avaliadas as folhas totalmente expandidas e completamente maduras, coletando as variáveis: taxa fotossintética líquida por unidade de área foliar (A, μmol CO2 m-2 s-1), condutância estomática ao vapor d’água (gs, mol H2O m-2 s-1), a taxa transpiratória (E, mmol H2O m-2 s-1) e a concentração interna de CO2 (Ci).
Foram realizadas medidas biométricas de crescimento através da medição da altura da parte aérea (AP), utilizando régua graduada (cm) a partir do substrato até a gema apical e diâmetro do coleto (D), medido com o auxílio de um paquímetro digital, ao nível do substrato.
Em cada coleta destrutiva todas as plantas foram divididas em raiz, caule e folhas sendo acondicionadas em sacos de papel e secas em estufa de ventilação forçada de ar a 75 °C até peso constante. Em seguida, foram pesadas em balança semi-analítica para obtenção da massa seca de folhas (MSF), massa seca de caule (MSC), massa seca de raíz (MSR), massa seca da parte aérea (MSPA) e massa seca total (MST).
O delineamento experimental utilizado foi inteiramente casualizado com dois tratamentos: plantas irrigadas e não irrigadas, com 9 plantas cada, considerando cada planta como uma repetição, sendo estes tratamentos repetidos em 3 tempos (0, 5 e 9 dias), totalizando 27 plantas por tratamento.
Os resultados obtidos foram analisados estatisticamente sendo submetidos à análise de variância e a diferença significativa entre as médias foram determinadas pelo teste F ao nível de 5% de probabilidade. O programa utilizado foi o JMP 4.0 (SAS Institute, 2008).
As variáveis de fotossíntese (A), condutância estomática (gs), e transpiração (E) foram significativamente reduzidas com a suspensão da disponibilidade de água no solo (Figura 1), tendo aumento apenas para concentração interna de CO2 (Ci), havendo interação estatística significativa da suspensão hídrica. Quando comparado com as plantas controle, os valores de A diminuíram de 4,85 para 0,39 µmol m-2 s-1 (Figura 1a), em média, correspondendo em termos percentuais 92%, acompanhando o mesmo ritmo a transpiração (E) de 1,60 para 0,45 mmol m-2 s-1 (Figura 1b), essa redução representou 72%. Para a gs a redução foi de 0,12 para 0,02 mol m-2 s-1 (Figura 1c), enquanto que as Ci aumentou de 236,97 para 376,58 m mol mol-1 (Figura 1d).
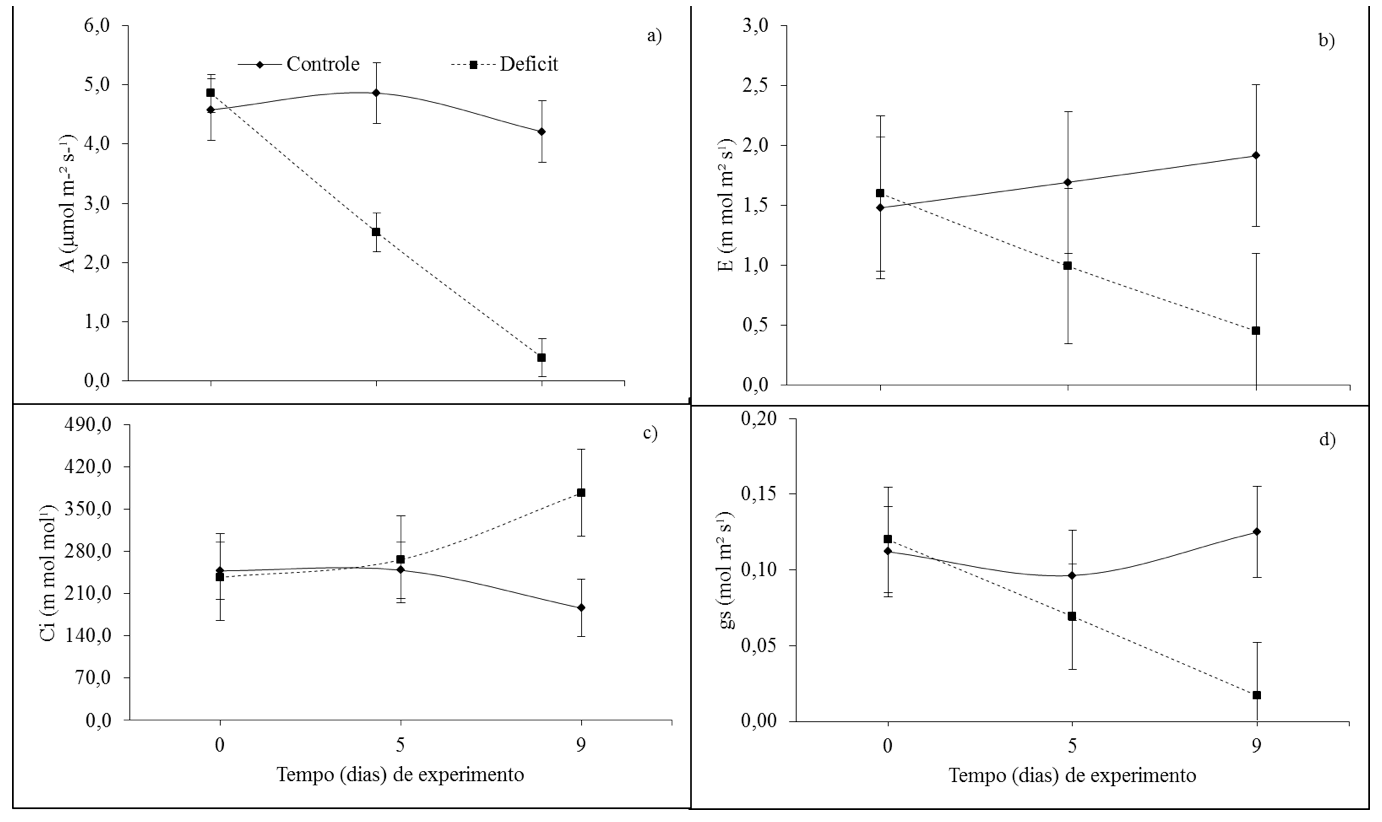
Figura 1 . Trocas gasosas das plantas irrigadas (controle) e não irrigadas (déficit hídrico),
a) fotossíntese; b) transpiração; c) concentração interna de CO2 e d) condutância estomática.
Maes (2009) encontrou em plantas jovens de Jatropha curcas valores de A e E que chegaram próximos a zero com a aplicação do estresse hídrico. Gonçalves et al., (2009) verificaram reduções em 88 e 89% na taxa fotossintética e transpiração respectivamente, após 21 dias de deficiência hídrica em plantas de andiroba comparadas com plantas irrigadas diariamente.
Em condições de déficit hídrico as plantas normalmente apresentam um decréscimo paralelo de A e gs. Um rápido fechamento estomático pode estar associado a uma rápida adaptação das plantas ao estresse hídrico (ROZA, 2010).
Embora o fechamento estomático seja uma resposta comum ao estresse hídrico, espécies diferentes podem apresentar comportamentos distintos de sensibilidade e taxas de resposta. De acordo com os trabalhos realizados por Tatagiba et al. (2007) e Otto et al. (2013), em clones de eucalipto, aos quais alcançaram valores distintos de condutância estomática, e ambos tiveram suas condutâncias reduzidas na época seca, demonstrando que o eucalipto exerce controle estomático eficiente em condições de suprimento hídrico no solo limitado.
A variação proporcional de A e gs, possibilita que a concentração interna de CO2 (Ci) se mantenha constante com o intuito de otimizar as trocas gasosas. O aumento de A está diretamente relacionado à diminuição da limitação estomática. Quando valores de Ci aumentam com o aumento de gs, a limitação estomática seria o fator principal da limitação do desempenho fotossintético, uma vez que quanto maior a abertura estomática maior a difusão de CO2 para a câmara subestomática (SANTOS et al., 2013).
Quando ocorre aumento na concentração interna de CO2 (Ci) com diminuição de gs, em condições de deficiência hídrica, o decréscimo de “A” indica que esta limitação é devida não somente ao aumento da resistência estomática, mas, também, ao efeito do estresse hídrico sobre a “A”, visto que um alto valor de Ci, associado aos baixos valores de gs, indicaria um decréscimo na eficiência de carboxilação (ROZA, 2010; SANTOS et al., 2013). Alguns autores atribuem a manutenção aproximadamente constante de Ci, durante o estresse hídrico, a valores desuniformes de gs ao longo do mesofilo, no entanto, esta heterogeneidade não é comum a todas as espécies, principalmente quando o estresse é imposto lentamente (MAES et al., 2009; ROZA, 2010; SANTOS et al., 2013).
Roza (2010) sugere que o aumento de Ci, sob baixa disponibilidade hídrica, pode estar relacionado à queda na atividade de enzimas envolvidas no processo de fixação de CO2. Fatores não estomáticos, como redução da atividade e concentração da enzima Ribulose 1-5 bifosfato carboxilase/ oxigenase (Rubisco), fotoinibição, taxa de transferência de elétrons e redução da eficiência fotoquímica de FS 2, em condições de estresse hídrico podem prejudicar a fotossíntese (DEUNER et al., 2011; BRITO et al., 2012; MARTINAZZO et al., 2013). Em Attalea funifera também foram observados aumento de Ci em baixos valores de gs (NASCIMENTO, 2009).
Para as respostas de crescimento, de acordo com a análise de variância das variáveis D e AP, verificou-se efeito significativo apenas para D, ao qual aos 9 dias foi observado um aumento médio de 16,98 de diâmetro nas plantas irrigadas quando comparado as não irrigadas (16,44 mm) (Tabela 2), mostrando que a falta de água na planta limitou seu crescimento em diâmetro.
Tabela 1. Teste de médias das variáveis: Diâmetro do Coleto (D); Altura de Plantas (AP);
Massa Seca de Folha (MSF); Massa Seca de Caule (MSC); Massa Seca de Raiz (MSR);
Massa Seca da Parte Aérea (MSPA) e Massa Seca Total (MST) das plantas controle
(tratamento irrigado) e sob déficit hídrico (tratamento não irrigado).
IRRIGADO |
|||||||
Tempo (dias) |
D(mm) |
AP (cm) |
MSF (g) |
MSC (g) |
MSR (g) |
MSPA (g) |
MST (g) |
0 |
16,67 Aa |
112,00 Aa |
22,01 Aa |
67,46 Aa |
69,62 Aa |
89,47 Aa |
159,09 Aa |
5 |
16,79 Aa |
112,12 Aa |
23,01 Aa |
68,46 Aa |
70,62 Aa |
91,47 Aa |
162,09 Aa |
9 |
16,98 Aa |
112,73 Aa |
24,59 Aa |
70,05 Aa |
72,20 Aa |
94,64 Aa |
166,84 Aa |
NÃO IRRIGADO |
|||||||
Tempo (dias) |
D (mm) |
AP (cm) |
MSF (g) |
MSC (g) |
MSR (g) |
MSPA (g) |
MST (g) |
0 |
16,17 Aa |
111,89 Aa |
22,07 Aa |
45,10 Aa |
73,70 Aa |
67,17 Aa |
140,87 Aa |
5 |
16,29 Bb |
112,01 Aa |
23,07 Aa |
46,10 Bb |
74,70 Aa |
69,17 Bb |
143,87 Bb |
9 |
16,44 Bc |
108,09 Aa |
24,66 Aa |
46,68 Bc |
76,29 Aa |
71,34 Bc |
147,63 Bc |
Médias seguidas de letras maiúsculas na mesma coluna diferem significativamente entre
os tratamentos e médias seguidas de letras minúsculas na mesma coluna diferem entre os
dias de experimento, ao nível de 5% de probabilidade.
A perda acentuada de água reduz a multiplicação e o alongamento das células, resultando em plantas com menores alturas (JALEEL et al., 2009; ROZA, 2010). Isso pôde ser observado por (ACHTEN et al., 2010) quando trabalharam com a espécie Jatropha curcas sob estresse hídrico obtiveram um decréscimo para a variável altura de 90 cm para 50 cm. Porém a castanheira-do-brasil não houve diferenças estatísticas significativas para o parâmetro de crescimento em altura, isto pode estar relacionado ao curto período de tempo que as plantas atingiram o pico de estresse hídrico (condutância próxima a zero) aliado ao lento ritmo de desenvolvimento da espécie. Segundo SCOLES et al. (2011) a castanheira-do-brasil tem incremento médio anual maior que 1m, o que representa cerca de 0,28 centímetro ao dia.
Houve redução significativa da MSC e MST (Tabela 2), demonstrando que a suspensão hídrica limitou o alongamento celular das plantas de castanheira-do-brasil. Schwider, et al. (2013) observaram que o acúmulo de massa seca total de eucalipto é reduzido em ambientes que apresentam baixa disponibilidade de água.
A massa seca de raiz foi moderadamente aumentada (Tabela 2) com a suspensão hídrica das plantas, embora a produção de matéria de massa seca das raízes das plantas que sofreram suspensão hídrica, não tenham apresentado interação significativa, podendo a não significância está relacionada ao curto período de tempo em que as plantas apresentaram estresse fisiológico, não sendo este tão expressivo na parte vegetativa, devido ao lento crescimento da espécie pois, segundo Salomão et al. (2014), as espécies de castanheira-do-brasil apresentam incremento médio anual em diâmetro maior que 3 cm e incremento médio anual em altura de 2 m.
A condição de deficiência hídrica por nove dias afetou adversamente o crescimento e os indicadores de trocas gasosas (A, gs e E). A condição de deficiência hídrica por nove dias, ao contrário, aumentou a concentração interna de CO2.
ACHTEN, W. M. J.; et al. Biomass production and allocation in Jatropha curcas L. seedlings under different levels of drought stress. Biomass and Bioenergy, v. 3 4, n. 5, p. 667–676, 2010.
AZEVEDO, G. F. da C. Photosynthetic parameters and growth in seedlings of Bertholletia excelsa and Carapa guianensis in response to pre-acclimation to full sunlight and mild water stress. Acta Amazonica. v. 44, n.1 p. 67-77, 2014.
BRITO, M.; et al. Comportamento fisiológico de combinações copa/porta-enxerto de citros sob estresse hídrico. Revista Brasileira de Ciências Agrárias, v.7, p.857-865, 2012.
COSTA, J. R.; et al. Aspectos silviculturais da castanha-do-brasil (Bertholletia excelsa) em sistemas agroflorestais na Amazônia Central. Acta Amazonica, v. 39, n. 4, p. 843-850, 2009.
DEUNER, S.; et al. Stomatal behavior and components of the antioxidative system in coffee plants under water stress. Scientia Agricola, v. 68, n. 1, p. 77-85, 2011.
FERREIRA, M. J.; GONÇALVES, J. F. de C.; FERRAZ, J. B. S. Crescimento e eficiência do uso da água de plantas jovens de castanheira-da-amazônia em área degradada e submetidas à adubação. Ciência Florestal, v. 22, n. 2, p. 393-401, 2012.
GASPARIN, E.; et al. Influência do substrato e do volume de recipiente na qualidade das mudas de Cabralea canjerana (Vell.) Mart. em viveiro e no campo. Ciência Florestal, v. 24, n. 3, p. 553-563, 2014.
GOMES, I. B. Respostas ecofisiológicas de plantas jovens de Bertholletia excelsa H. B. submetidas à fertilização em plantio homogêneo. 2012. 59 f. Dissertação (Mestrado em Ciências de Florestas Tropicais) - Instituto Nacional de Pesquisas da Amazônia (INPA), 2012.
GONÇALVES, J. F. de C.; SILVA, C. E. M. da; GUIMARÃES, D. G. Fotossíntese e potencial hídrico foliar de plantas jovens de andiroba submetidas à deficiência hídrica e à reidratação. Pesquisa Agropecuária Brasileira, v.44, n.1, p.8-14, 2009.
HAUGAASEN, J. M. T.; HAUGAASEN, T.; PERES, C. A.; GRIBEL, R.; WEGGE, P. Fruit Removal and Natural Seed Dispersal of the Brazil Nut Tree (Bertholletia excelsa) in Central Amazonia, Brazil. Biotropica, v. 44, n. 2. p.205–210, 2012.
HAUGAASEN, J. M.; HAUGAASEN, T.; PERES, C. A.; GRIBEL, R.; WEGGE, P. Seed dispersal of the Brazil nut tree (Bertholletia excelsa) by scatter-hoarding rodents in a central Amazonian forest. Journal of Tropical Ecology, v. 26, n. 3, p. 251–262, 2010.
JALEEL, C. A.; et al. Drought Stress in Plants: A Review on Morphological Characteristics and Pigments Composition. International Journal Agricultural Biology, v. 11, n. 1, p. 100–105, 2009.
MAES, M. H.; et al. Plant–water relationships and growth strategies of Jatropha curcas L. saplings under different levels of drought stress. Journal of Arid Environments, v. 73, n. 10, p. 877–884, 2009.
MARTINAZZO, E. G.; et al. Atividade fotossintética em plantas de ameixeira submetidas ao déficit hídrico e ao alagamento. Ciência Rural, v. 43, n. 1, p. 35-41, 2013.
MORAIS, R. R.; et al. Chloroplastid pigment contentas and chlorophyll a fluorescence in Amazonian tropical three species. Revista Árvore, v.31, n.5, p. 959-966, 2007.
NASCIMENTO, J. L. do. Crescimento e assimilação de carbono em plantas jovens de Attalea funifera Mart. submetidas ao sombreamento e ao estresse hídrico. 2009. 97 f. Dissertação (Mestrado em Produção Vegetal) – Universidade Estadual de Santa Cruz. Ilhéus – Bahia, 2009.
OTTO, M. S. G.; et al. Fotossíntese, condutância estomática e produtividade de clones de Eucalyptus sob diferentes condições edafoclimáticas. Revista Árvore, v. 37, n. 3, p. 431-439, 2013.
ROZA, F. A. Alterações morfofisiológicas e eficiência de uso da água em plantas de Jatropha curcas L. submetidas à deficiência hídrica. 2010. 67 f. Dissertação (Mestrado em Produção Vegetal) – Universidade Estadual de Santa Cruz. Ilhéus – Bahia, 2010.
SALOMÃO, R. de P.; et al. Crescimento de Bertholletia excelsa Bonpl. (castanheira) na Amazônia trinta anos após a mineração de bauxita. Boletim do Museu Paraense Emílio Goeldi. Ciências Naturais, Belém, v. 9, n. 2, p. 307-320, 2014.
SANTOS, M. R. dos; MARTINEZ, M. A.; DONATO, S. L. R. Gas exchanges of ‘tommy atkins’ mango trees under different irrigation treatments. Bioscience Journal, v. 29, n. 5, p. 1141-1153, 2013.
SAS Institute. User’s guide. Version 9.2. Cary, NC: SAS Institute Inc. 584pp. 2008.
SCHWIDER, Y. S.; et al. Efeito do déficit hídrico sobre o crescimento de eucalipto em diferentes condições microclimáticas. Enciclopédia Biosfera, v.9, n.16; p. 888-900, 2013.
SCOLES, R.; GRIBEL, R.; KLEIN, G. N. Crescimento e sobrevivência de castanheira (Bertholletia excelsa Bonpl.) em diferentes condições ambientais na região do rio Trombetas, Oriximiná, Pará. Boletim do Museu Paraense Emílio Goeldi. Ciências Naturais, v.6, n.3, p. 273-293, 2011.
SUJII, P.S.; et al. Morphological and molecular characteristics do not confirm popular classification of the Brazil nut tree in Acre, Brazil. Genetics and Molecular Research, v. 12, n. 3, p. 4018-4027, 2013.
TATAGIBA, S. D.; et al. Comportamento fisiológico de dois clones de Eucalyptus na época seca e chuvosa. Revista Cerne, v. 13, n. 2, p. 149-159, 2007.
TONINI, H. Fenologia da castanheira-do-Brasil (Bertholletia excelsa Humb. & Bonpl., Lecythidaceae) no sul do estado de Roraima. Revista Cerne, v. 17, n. 1, p. 123-131, 2011.
1. Doutorando em Ciências Florestais. Programa de Pós-Graduação em Ciências Florestais. Universidade Federal Rural da Amazônia. Belém-Pa. E-mail: eng.lenilson@gmail.com
2. Doutor em Biologia Vegetal Fisiologia Vegetal. . Professor do Instituto de Ciências Agrárias. Universidade Federal Rural da Amazônia. Belém-Pa. E-mail: benedito.filho@ufra.edu.br
3. Mestre em Ciências Florestais. Centro de Ciências Naturais e Tecnologia. Universidade do Estado do Pará. Belém-PA. E-mail: simoes.florestal@gmail.com
4. Doutorando em Ciências Florestais. Programa de Pós-Graduação em Ciências Florestais. Universidade Federal Rural da Amazônia. Belém-Pa. E-mail: glauand@yahoo.com.br
5. Doutor em Ciências Agrárias. Professor do Instituto de Ciências Agrárias. Universidade Federal Rural da Amazônia. Belém-Pa. E-mail: candido.neto@ufra.edu.br
6. Graduando em Engenharia Florestal. . Universidade Federal Rural da Amazônia. Belém-Pa. E-mail: ruanferreira55@hotmail.com