

Vol. 38 (Nº 14) Año 2017. Pág. 24
Lethícia MALLET Vivas 1; Maria Clara LIPPI 2; Guido Vaz SILVA 3; Leonardo Luiz Lima NAVARRO 4; Adriano PROENÇA 5
Recibido: 27/09/16 • Aprobado: 12/10/2016
RESUMO: O presente artigo trata do conceito Pesquisa Translacional, que tem demonstrado relevância como um instrumento potencial para acelerar a inovação tecnológica e aproximar resultados de pesquisas básicas com aplicações eficazes no atendimento das demandas de saúde. Nesse sentido, o objetivo desta pesquisa consiste em explorar o potencial da abordagem da pesquisa translacional como perspectiva de interesse da Engenharia de Produção na análise da integralidade de cadeias produtivas (do P&D ao consumo) de medicamentos. Para tal, realizou-se uma revisão sistemática da literatura que suportou a identificação de gaps na cadeia produtiva de medicamentos com comportamentos dinâmicos e não-lineares. |
ABSTRACT: This article is about the concept of Translational Research as a potential approach to accelerate technological innovation and bring basic research results to effective applications on health demands. This research explores Translational Research as a subject of interest of Industrial/Production Engineering in the analysis of pharmaceutical drugs’ productive chains (from R&D to consumption). For this purpose, the autors proceeded a systematic literature review and identified gaps in the pharmaceutical drugs’ supply chain considering its dynamic and non-linear behaviors. |
O conceito da Pesquisa Translacional (PT) não é novo. Segundo Wehling (2006) alguns termos bem conhecidos no presente já foram usados no passado reunindo expectativas similares as da Pesquisa Translacional, como por exemplo, “Pesquisa Clínica”, “Pesquisa Aplicada, “Pesquisa Baseada em Evidências”. Hoje os termos comuns são “Medicina Translacional”, “Ciência Translacional” e “Pesquisa Translacional”. A base indexada PubMed, através do MeSH (Medical Subject Headings), situa a PT como subárea da Pesquisa Biomédica, considerando o termo “pesquisa médica translacional” (ou translational medical research), cuja definição é a seguir transcrita:
A aplicação das descobertas geradas por pesquisas de laboratório e estudos pré-clínicos para o desenvolvimento de ensaios clínicos e estudos em seres humanos. Uma segunda área de preocupação da pesquisa translacional reforça a adoção das melhores práticas. (PubMed, 2012).
A escolha do termo “Pesquisa Translacional” por este trabalho procura acompanhar a adoção recorrente pela literatura recente na área, e também a coerência teórica do termo. Há inadequações em relação às demais expressões. O termo “Medicina translacional” restringe as aplicações e estudos para o campo Biomédico, negligenciando a característica interdisciplinar da abordagem translacional. E a expressão “Ciência Translacional” é considerada prematura para tratar de uma área bastante recente e ainda em conformação.
A relevância da Pesquisa Translacional (PT) não está em seu objeto em si, mas sim na ênfase dedicada à urgente necessidade de identificar e solucionar os problemas que minam a transferência efetiva do avanço científico em conhecimento aplicado e útil (Wehling, 2010). A nova disciplina surge de um contexto de superespecialização e consequente fragmentação das atividades de pesquisa biomédica, que trazem a necessidade de maior comunicação entre as áreas básica e clínica (Wehling, 2010).
Parte dos autores adota a definição de que a PT é representada ao longo das etapas clássicas do processo de desenvolvimento tecnológico, sintetizada pela expressão “da bancada ao leito”, que considera parte do escopo da Pesquisa Translacional inclusive os estudos da pesquisa básica para descoberta de novas moléculas focando na sua transição para aplicações clínicas seguras (Curry, 2008, Coller; Callif, 2009, Collins, 2011). Por outro lado, há uma segunda corrente na literatura que trata por este termo todo o escopo que abrange a cadeia (do P&D ao consumo) de um novo medicamento, desde as descobertas de novas drogas potenciais realizadas na pesquisa básica e testadas na pesquisa clínica até a difusão de medicamentos efetivos e seguros para a população (Trochim et al., 2011; Palinkas; Soydan, 2012).
A incorporação destas etapas de pré e pós desenvolvimento tecnológico se dá a partir da evolução do entendimento do processo translacional sob uma perspectiva sistêmica da inovação em saúde, da descoberta ao paciente (Guimarães, 2013). Esta pesquisa, portanto, adota a definição trazida por Alving et al. (2012), a qual entende a Pesquisa Translacional como um conjunto de esforços empregados para transferir os resultados obtidos desde a pesquisa básica até a adoção e consumo por parte dos usuários/pacientes, tendo como fim o atendimento de uma necessidade de saúde, e como premissa a interdependência e integração permanentes entre as etapas da cadeia produtiva.
Hoje, existem diferentes modelos aplicáveis à análise do processo translacional. Estes variam segundo o nível de fragmentação proposto para os gaps (momentos de translação considerados críticos) da cadeia de uma nova droga (Trochim et al, 2011). Desta forma, o objetivo desta pesquisa consiste em explorar o potencial da abordagem da pesquisa translacional, em especial os modelos de análise do processo translacional, como perspectiva de interesse da Engenharia de Produção na análise da integralidade de cadeias produtivas (do P&D ao consumo) de medicamentos. A questão de pesquisa a ser respondida é: Como a utilização da abordagem translacional pode potencializar a representação e análise de cadeias produtivas de medicamentos, na direção de efetivar melhores resultados na adoção e acesso por parte do usuário/paciente?
Com origem nos Estados Unidos, a Pesquisa Translacional teve rápida expansão para os demais países desenvolvidos e em desenvolvimento, a partir da sua “promessa” de desvendar os gargalos do processo de inovação tecnológica em novos medicamentos e terapias, a partir de uma nova perspectiva de análise do problema.
Basicamente, a abordagem pela Pesquisa Translacional deveria ser capaz de acelerar o tempo de atravessamento desde uma descoberta até em uma nova droga acessível (Wehling, 2010, Trochim et al, 2011, Palinkas; Soydan, 2012, Guimaraes, 2013). Sua abordagem interdisciplinar está orientada a uma espécie de “reengenharia” da cadeia de desenvolvimento de novas drogas (National Institutes of Health, 2006, Zerhouni, 2006, Woods; Magyary, 2010), com o sentido de ser instrumento potencial para acelerar a inovação tecnológica na área da saúde.
Observa-se, portanto, a necessidade de se desenvolver um adequado enquadramento do problema, passando pela exploração de uma nova perspectiva de análise que enxergue de maneira integral a cadeia (considerando toda sua amplitude). Nesse sentido, este tópico apresenta um contraponto entre o panorama teórico-prático da PT (2.1) e as abordagens vigentes para representação e entendimento de cadeias produtivas no setor de saúde (em especial, do farmacêutico. São elas: a cadeia de valor (2.2), a cadeia de suprimentos (2.3) e a rede de agentes (2.4). O resultado evidencia contribuições importantes da PT para gaps identificados na literatura de cadeias produtivas aplicadas ao setor farmacêutico.
Para compreender melhor a abordagem da Pesquisa translacional (PT) é necessário avaliar em que bases teórico-práticas históricas ela se encontra fundamentada. Para isso, é necessário analisar dois fenômenos principais – o movimento da Medicina Baseada em Evidências (MBE) e o lançamento do Roadmap de Pesquisa em Medicina, pelo Instituto Nacional de Saúde dos Estados Unidos (National Institutes of Health - NIH).
A MBE foi um movimento em saúde, oriundo das Ciências Biomédicas, baseado na integração entre a experiência clínica (do pesquisador e médico) com a melhor evidência clínica externa, fundamentada em revisões sistemáticas rigorosas, especialmente levando em consideração as circunstâncias (valores e expectativas) do paciente, denominada por “tríade da MBE" (Sackett et al., 1996; Strauss et al., 2011).
A MBE foi de fundamental importância para que a discussão da Pesquisa Translacional ganhasse corpo e peso nas comunidades acadêmicas e profissionais, tendo em vista ser o objetivo da PT aproximar os elos da tríade da MBE (Palinkas; Soydan, 2012), materializando a necessidade de tratar o gap inicialmente identificado entre o pesquisador básico e o pesquisador clínico. Ou seja, entre o conhecimento de base científica e a inovação na área da saúde, criando as “pontes” entre a pesquisa e a prática mencionadas por Curry (2008), Coller; Califf (2009), Fitzgerald (2010a), Fitzgerald (2010b), Collins (2011), Silva (2014), e outros.
Sob este contexto, o Instituto Nacional de Câncer dos Estados Unidos (NCI) é datado como pioneiro no estudo e investimento intensivos na PT (em 1992), com o intuito de aproximar a pesquisa básica da pesquisa clínica, em uma via bidirecional e integrada (Guimaraes, 2013).
Com o diagnóstico de que as estruturas de pesquisa (Institutos de C&T, Hospitais e Universidades) estavam em desarmonia com a prática clínica e a indústria, o NIH lançou um Roadmap de Pesquisa em Medicina, em 2003, onde priorizava áreas centrais de ação para resolução das questões de saúde. Uma das áreas de ação constantes do documento é centrada na “Reengenharia da Iniciativa em Pesquisa Clínica”, representada pela adesão à então chamada Pesquisa Translacional – aquela que se ocupa de investigar a tradução de uma descoberta científica em um novo medicamento (Curry, 2008; National Institutes of Health, 2006).
Como desdobramento da linha de “Reengenharia da Iniciativa em Pesquisa Clínica”, em 2006, o NIH lançou o programa CTSA (Clinical and Translational Science Award), linha de fomento institucional vinculada especificamente à construção de uma ponte entre o pesquisador básico e o clínico, dentro das instituições de pesquisa norte-americanas em Medicina.
Em 2012 foi criada uma nova unidade do NIH, dedicada ao suporte a iniciativas de criação de centros de pesquisa focados em PT (o National Center for Advancing Translational Sciences - NCATS), com o intuito de estimular a aproximação das duas pontas do “vale da morte”, articulando as iniciativas de pesquisa com mecanismos regulatórios, redes de colaboração, entre outros (Collins, 2011, Coller; Califf, 2009). O “vale da morte” é conceituado, por sua vez, como o gap existente entre o momento de descoberta de uma potencial aplicação clínica e a comprovação de sua segurança e eficácia em humanos (Coller; Califf, 2009, Califf; Berglund, 2010).
Nesse contexto, a chamada Pesquisa Translacional ganha proeminência internacional, e emerge com força no debate internacional em Saúde (Collins, 2011, Coller; Califf, 2009), se expandindo para todo o conjunto de atividades existentes entre a descoberta oriunda da pesquisa básica e a sua conversão em aplicação para a população na prática médica (Trochim et al., 2011). Da maneira mais agregada e simplificada, a Figura 1 apresenta a trajetória da Pesquisa Translacional quanto à amplitude de seu escopo, que passa a incorporar em uma visão mais contemporânea, outras etapas da cadeia da inovação para além do “ vale da morte”, ao se perceber que uma inovação só se concretiza se é capaz de ser disseminada e adotada pelo usuário/paciente.
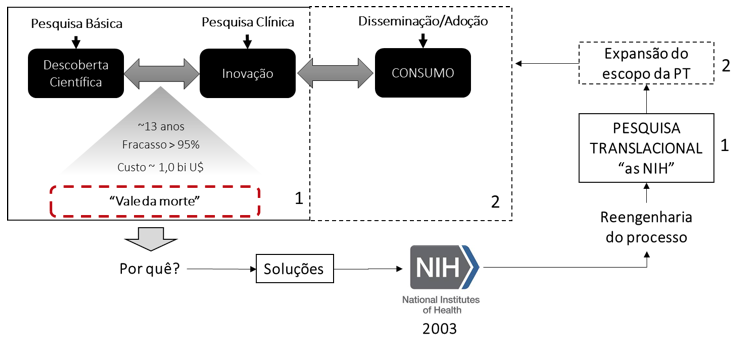
Figura 1: Trajetória simplificada da extensão do escopo da Pesquisa Translacional
Chiesa & Chiaroni (2005) apresentam um modelo conceitual adaptado da cadeia de valor para o caso farmacêutico, como uma cadeia que vai da descoberta de uma nova droga até os testes pós comercialização. Dividem as principais atividades da cadeia pelo momento que precede a aprovação da agência reguladora, e o momento pós aprovação para comercialização (Figura 2).
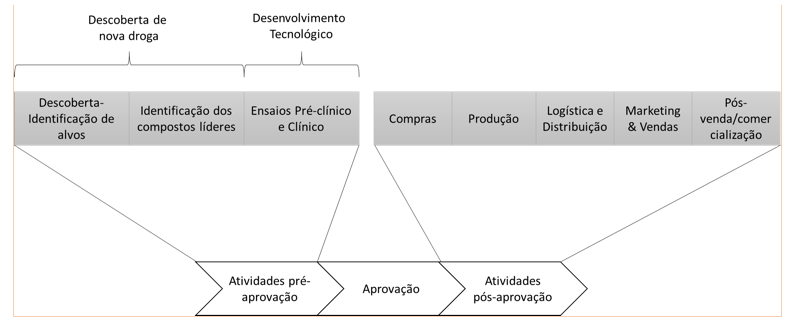
Figura 2: Cadeia de valor farmacêutica. Fonte: Adaptado de Chiesa & Chiaroni (2005)
O momento prévio à aprovação inclui as atividades de pesquisa química e biológica para identificação de novos compostos com potenciais aplicações clínicas para alvos específicos relacionados a certa doença. O composto ou os compostos líderes identificados se revertem em drogas “candidatas”, que passam então para a etapa de desenvolvimento tecnológico propriamente dito, onde o protótipo da nova droga será conduzido por ensaios não clínicos (em animais) e, caso aprovada por agência reguladora pertinente, é transferida para os ensaios clínicos em seres humanos (Fases I, II e III) (Chiesa & Chiaroni, 2005).
A cada fase do ensaio clínico o grupo de pessoas aumenta. Na Fase I o objetivo é testar a segurança da potencial droga; na fase II a sua eficácia, e na Fase III para verificar eficácia, segurança e custo benefício em escala. A fase IV se inicia após a aprovação da Fase III, e já se direciona ao acompanhamento dos efeitos da droga no mercado (farmacovigilância).
Quanto ao uso da cadeia de valor como modelo, percebe-se, em primeiro lugar, uma certa aproximação simplificada do modelo original, já que as atividades nomeadas como primárias e secundárias preconizadas por Porter (1985) não são explicitamente discriminadas. Em segundo lugar, a representação não consegue explicitar, entre outros fatores:
A análise pela cadeia de valor agrega conhecimento e é importante para o primeiro momento de ambientação com as atividades investigadas. No entanto, a localização de questões críticas ao longo do processo, e notadamente em suas interfaces, não é possibilitada no nível de simplificação adotado por este modelo.
Kazemzadeh et al.(2012) apresentam uma cadeia de suprimentos genérica de medicamentos onde os agentes são dispostos segundo a natureza das atividades que realizam (Figura 3).
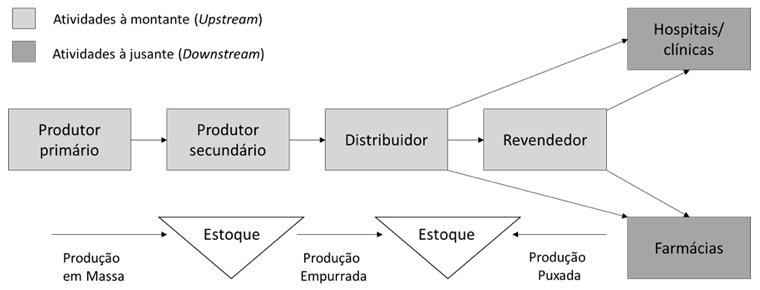
Figura 3: Estrutura simplificada da cadeia de suprimentos da Saúde. Fonte: Adaptado de Kazemzadeh et al.(2012)
De maneira geral, os atores a montante (em cinza claro) realizam atividades ligadas ao desenvolvimento e produção do princípio ativo contido no medicamento (produtor primário) e a produção do medicamento propriamente dito (produtor secundário) com as atividades logísticas relacionadas à distribuição e revenda. À jusante (em cinza escuro) concentram-se os atores relacionadas à entrega do medicamento ao usuário na ponta – os hospitais, clínicas, farmácias e outros.
Há limitações evidentes (à parte da simplificação para representação) quanto à incorporação das atividades de pesquisa e desenvolvimento tecnológico (DT) (mais bem colocadas na representação da cadeia de valor), por exemplo. O produtor primário (ou fabricante do Insumo Farmacêutico Ativo) pode realizar DT, mas é pouco provável. Não raro na literatura, estas conexões, em se tratando da cadeia de suprimentos, ficam superficiais, sendo apenas indicadas como relevantes do ponto de vista da estratégia competitiva, ou sendo simplesmente negligenciadas (Rees, 2011).
E ainda, na linha de pensamento de Jaberidoost et al.(2013), Adner (2012) e Baxter et al.(2013), como a cadeia de suprimentos trataria problemas relativos à adoção de um determinado produto? Se o usuário não é visto como co-inovador na chamada “cadeia de adoção” (Adner, 2012) de um novo produto, a cadeia de suprimentos irá entregar o produto, porém este não será de fato consumido.
Por outro lado, Christopher (1998) entende que a cadeia de suprimentos é uma rede de organizações interligadas a jusante e a montante por atividades que geram serviços e produtos imbuídos de valor ao usuário final. Lambert et al.(1998) defende, ainda, que tais relações não se limitam a formas lineares “um para um”, mas podem se expandir em conexões múltiplas, como colocam.
Em síntese, percebe-se que os trabalhos atuais em Gestão da Cadeia de Suprimentos de Medicamentos focam, principalmente, no tratamento de classes de problemas mais ou menos definidas – Planejamento e Controle da Produção (PCP), Gestão de Estoques, Logística de Distribuição, entre outros. Em geral, são questões a serem resolvidas dentro de cada organização, para que toda a rede de agentes da cadeia possa funcionar de maneira integrada.
No entanto, a preocupação desta pesquisa não reside de imediato nestas classes de problemas da escola tradicional. A preocupação central encontra-se na classe de problemas presente nas interfaces ou momentos de transição do produto/terapia ao longo da cadeia e, que eventualmente, estarão relacionadas a esta natureza de problemas mais clássica. O interesse está mais nas conexões do que necessariamente nas unidades/elos.
Neste sentido, caminha-se de maneira mais aproximada para a definição de cadeia de suprimentos que remete à teia ou rede de relacionamentos associados à realização de atividades-chave, pelo foco que esta abordagem conceitual traz às ligações entre os agentes e entre as atividades essenciais. Rees (2011) ratifica esta ideia ao observar que esta configuração em rede vem se transformando cada vez mais no novo desenho das cadeias de suprimento, conforme discutido no tópico 2.4.
Avançando para a relação da rede com a cadeia de suprimentos, Ford et al. (2003) mencionam os impactos diversos que uma pequena ação realizada por um agente pode ocasionar em outro, especialmente se as cadeias de suprimentos das quais fazem parte estiverem de alguma forma conectadas. Isto porque uma cadeia é em geral parte de uma rede composta por outras cadeias (Slack, Chambers, & Johnston, 2010). A rede é fruto de um conjunto de interações de caráter complexo entre organizações, onde as conexões estabelecidas entre as mesmas possuem significados específicos (Ford et al., 2003).
No âmbito da saúde, Baxter et al. (2013) estabelecem um sistema de redes denominado Navigating Ecosystem of Translacional Science (NETS) ou “Ecossistema de Navegação da Ciência Translacional”, um novo modelo de desenvolvimento de novas drogas que busca oferecer a implantação de um sistema aberto, colaborativo e transparente.
O modelo se baseia no pensamento sistêmico para visualizar o desenvolvimento tecnológico como parte de um todo, com a perspectiva de rede explicitada na interconexão entre os diversos processos/atividades que a compõem, permitindo fluxos circulares de feedback em detrimento do conjunto de passos discretos e lineares da cadeia de suprimentos padrão (Baxter et al., 2013).
O modelo NETS, no entanto, negligencia a parte da cadeia voltada à produção, seguindo a lógica da supervalorização do P&D na indústria farmacêutica descrita por Rees (2011). Inclusive, a presente pesquisa pretende avançar neste aspecto, considerando todas as etapas para a chegada ao usuário e os aspectos essenciais das conexões existentes entre essas etapas.
Este artigo é uma pesquisa bibliográfica, que contou com levantamento na literatura em três passos básicos: (i) busca extensiva; (ii) mapeamento sistemático da literatura; e (iii) processamento e seleção de textos. Os procedimentos metodológicos adotados para sua consecução são apresentados neste tópico.
Em um primeiro momento realizou-se uma busca extensiva ou busca de escopo em diversas bases para recolher, ainda de modo não estruturado ou sistemático, material inicial para imersão no assunto da pesquisa.
Após esta etapa de familiarização com o assunto da pesquisa houve refinamento das palavras-chave com base nas combinações (e resultados destas) realizadas na busca extensiva, tal qual indicado na Figura 4.
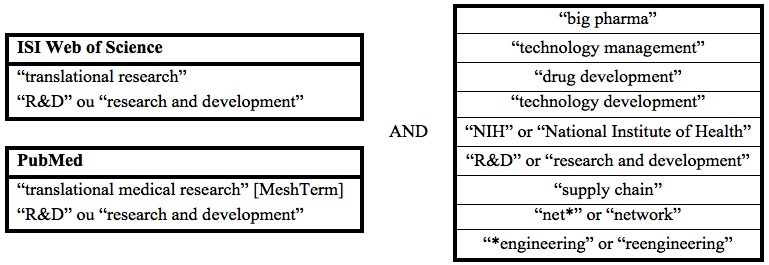
Figura 4: Palavras-chave utilizadas no mapeamento da literatura de Pesquisa Translacional
A partir daí conduziu-se ao mapeamento sistemático da literatura, por meio de busca intensiva nas bases consideradas pertinentes à revisão bibliográfica. Para algumas das publicações chave obtidas da revisão, realizou-se o método de raízes e ramos (Silva; Proença Jr., 2013), segundo as heurísticas “citado por” e “citando”, como uma forma de snowball tanto “para frente” como “para trás”. As bases de busca utilizadas foram a PubMed e a ISI Web of Science, além de busca por livros, na Amazon®, e teses, na Biblioteca Digital Brasileira de Teses e Dissertações (BDTD). Também foram incluídos e rastreados textos obtidos por indicação de pesquisadores próximos ao campo de estudo da PT.
Esta parte do levantamento bibliográfico foi bastante extensa, tendo em vista a quantidade de trabalhos em pesquisa translacional retornados. De modo geral, muitas publicações se repetiram de uma base para a outra, e dentro das bases percebeu-se, ainda, bastante recorrência nos assuntos e constatações. Desta forma, foi necessário filtrar inicialmente uma quantidade elevada de textos (título e resumo) considerados de assunto ou tema relevante.
Em um terceiro momento as obras levantadas no mapeamento da literatura começaram a ser processadas para seleção daquelas a integrarem o texto do documento. Na prática, o segundo filtro para leitura é que identificou as recorrências de conteúdo que não somavam, e permitiu um afunilamento maior dos textos considerados realmente relevantes para a pesquisa. Ou seja, a seleção de materiais iniciou com resultado bruto de busca de 1792 texto, finalizando, após os filtros de refinamento supracitados, em 53 materiais a serem explorados analiticamente para serem contemplados na presente pesquisa. Os resultados da busca considerados relevantes para esta pesquisa são sistematizados no tópico que segue.
Antes de apresentar os diferentes modelos translacionais propostos pela literatura de pesquisa translacional, cabe diferenciar a cadeia translacional da cadeia produtiva (do P&D ao consumo) de um medicamento. Há uma confusão recorrente neste sentido. Baumann et al. (2001) e Nordstrom (2007), por exemplo, entendem que as etapas translacionais são exatamente aquelas da cadeia de desenvolvimento tecnológico de uma droga, denominando a mesma como “cadeia da pesquisa translacional”, o que não procede.
Neste sentido, a Figura 5 diferencia as duas cadeias, evidenciando que a cadeia translacional se preocupa com as atividades que garantem a transição entre os gaps das etapas da cadeia de desenvolvimento e produção. Enquanto o medicamento é dito gerado pela cadeia produtiva, a cadeia translacional se ocupa em garantir o atravessamento fluido e ágil do produto entre as etapas consideradas críticas. Segundo Wehling (2010), a PT possui papel catalisador neste processo, como “uma enzima atuando em um substrato”.
Estas etapas, denominadas de modo simplificado como “Ts”, variam segundo o modelo translacional selecionado para análise da cadeia produtiva. Podem ser lidas como “momentos de translação”, “etapas de tradução” ou simplesmente “gaps translacionais”. Na Figura 5, o modelo exemplificado é o estratificado com quatro Ts (Khoury et al., 2007).
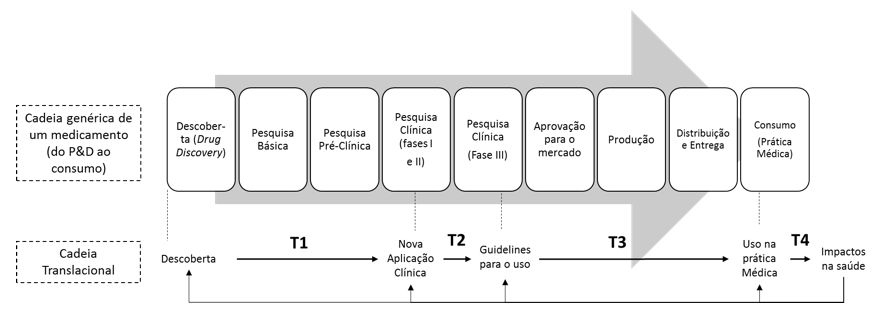
Figura 5: A cadeia translacional diante da cadeia produtiva do P&D ao consumo.
Fonte: Adaptado de Khoury et al. (2007)
Pode-se constatar que o critério de recorte de cada momento de translação T tem relação íntima com a divisão do trabalho entre agentes responsáveis pelas atividades da cadeia produtiva. O momento T1 indica a transição entre atividades de pesquisadores básicos para atividades de pesquisadores clínicos. O momento T2 indica a transição entre atividades do pesquisador clínico para atividades dos médicos (na definição de diretrizes e protocolos baseados em evidências) e dos agentes da indústria, interessados na produção e comercialização. T3 indica a passagem das atividades mercadológicas para aquelas da prática – interface entre a indústria e a comunidade médica que prescreve o medicamento. E, por fim, T4 marca a transição das atividades de incorporação pela comunidade médica na sua rotina de prescrição para os impactos sentidos pela população no consumo disseminado do produto. A Figura 6 detalha os modelos translacionais presentes na literatura compilados por Trochim et al. (2011).
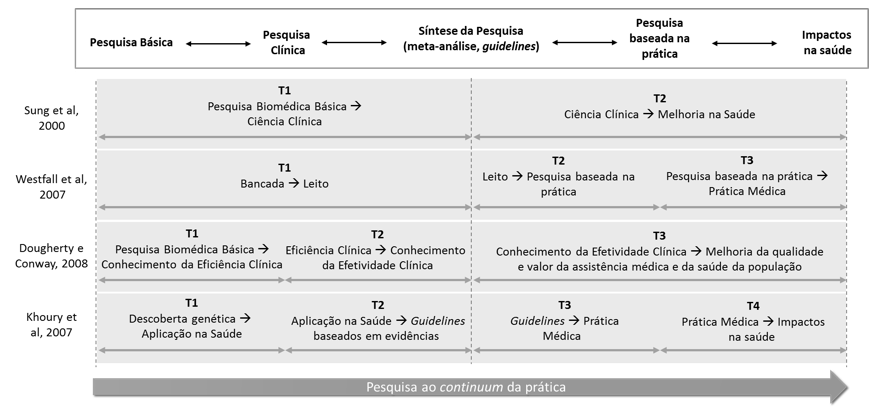
Figura 6: Conjunto dos modelos translacionais para análise de cadeias produtivas de medicamentos.
Fonte: Adaptado de Trochim et al. (2011)
Desta forma, os tópicos que seguem exploram o modelo dos 4Ts (Khoury et al., 2007), tendo em vista ser este o modelo mais recente, com escopo expandido gerado após curva de aprendizado iniciada em 2000. A estrutura do referido modelo é composta dos itens:
A pesquisa em T1 se inicia logo após a descoberta de uma nova molécula/composto e possui o objetivo de desenvolver uma aplicação candidata à utilização na prática clínica (Khoury et al., 2007). É a transferência da pesquisa básica para a pesquisa clínica, o chamado “vale da morte”, como amplamente tratado pela literatura no tema (Coller; Califf, 2009, Califf; Berglund, 2010).
As aplicações podem ser utilizadas para apoiar a avaliação clínica ou ainda para selecionar as melhores opções terapêuticas, e são realizadas a partir de estudos de observação, ensaios pré-clínicos e ensaios clínicos iniciais – fases 1 e 2 (Khoury et al., 2007).
Nesta etapa Wehling (2010) ressalta que não raramente o composto recém-descoberto é “lançado por sobre a cerca” para o departamento de desenvolvimento tecnológico. Esta expressão sinaliza a preocupação central da transferência de conhecimento ser realizada de maneira informada e integrada. O que ocorre muitas das vezes neste cenário, é que a pesquisa básica investiga de maneira independente da pesquisa aplicada. Estes dois grupos precisam estar orientados ao atendimento de demandas de saúde bem especificadas, e trabalhar em conjunto para alcançar compostos potenciais que persigam o atendimento dessas demandas.
Na etapa T1, as necessidades da saúde orientam as pesquisas, bem como o desenvolvimento de potenciais tratamentos terapêuticos (Bozza, 2011). Um exemplo da pesquisa translacional em T1 é o estudo e formatação de perfis genômicos – no âmbito da Medicina Personalizada – para orientar diretrizes futuras de intervenções clínicas perfil dependentes.
A etapa T2 corresponde à ampliação dos estudos clínicos e o desenvolvimento de protocolos baseados em evidências a partir da efetividade clínica da nova terapia/produto (Bozza, 2011). O resultado esperado para esta etapa é a revisão e síntese sistemática das evidências obtidas, que irão permitir e suportar a construção de protocolos de tratamento. Tendo em vista a dificuldade de se acumular e sistematizar as evidências, é comum que o período de tempo para sua conclusão adequada seja elevado (Khoury et al., 2007)
A formatação destes protocolos ou diretrizes baseadas em evidências se correlaciona com o fenômeno da EBM, preconizado pelas Ciências Biomédicas, para comprovação da possibilidade de uso e replicação do tratamento ou terapia na prática médica. Nesta etapa, não só os médicos e pesquisadores clínicos são envolvidos, mas ainda outros profissionais como estatísticos e epidemiologistas. (Khoury et al., 2007, Bozza, 2011).
Um problema averiguado por Khoury et al.(2007) nesta fase é que o processo de desenvolvimento destes guidelines baseados em evidência não é padronizado, e muitos são realizados a partir da opinião de um médico/pesquisador especialista no campo da medicina investigado.
Dentre outros impactos, destaca-se aqueles relativos à etapa de produção na cadeia produtiva, pouco abordada na literatura da Pesquisa Translacional. A ampliação dos ensaios clínicos (Fase III) deve considerar os desafios de adaptação para produção em escala piloto, e posteriormente à aprovação em escala industrial, já com protocolos clínicos estabelecidos a serem levados em consideração.
Um exemplo dos impactos nos protocolos é o da insulina recombinante (a ser detalhadamente exemplificada no próximo tópico). No momento da aprovação pelo órgão regulatório fez-se necessário a inclusão de um teste de função pulmonar não previsto pela empresa desenvolvedora, o que forçou uma mudança no protocolo clínico originalmente desenhado e que, por sua vez, poderia (ou não) mudar a escala de produção planejada para o medicamento, uma vez que menos pacientes passariam a acessar o tratamento (isto é, somente os que passassem no teste).
Uma vez registrados em protocolos clínicos baseados em evidências, é necessário fazer com que os médicos adotem o produto ou incorporem a nova terapia a sua rotina de cuidado com os pacientes (Khoury et al., 2007).
Adner (2012) oferece um exemplo bastante ilustrativo de um problema tipicamente do momento T3 referente ao desenvolvimento do Exubera pela Pfizer. Tratava-se da insulina pulmonar administrada por inalações, que melhoraria a qualidade de vida de milhões de pacientes diabéticos obrigados a administrar sua insulina através de injeções diárias. Chegando ao mercado, as vendas ficaram muito aquém do esperado, um total de US$ 12 milhões em vendas de uma expectativa de US$ 1,2 bilhões, o que fez a Pfizer descontinuar o produto. Vale ressaltar que o otimismo acerca do lançamento e da expectativa de vendas não era só da Pfizer, mas dos consultores especializados do mercado.
Todas as limitações já haviam sido previstas pela Pfizer desde os estudos pré-clínicos, e estratégias foram definidas para gerir e superar tais questões com antecedência (melhorias no dispositivo inalador, treinamento dos médicos e enfermeiros, etc.), porém um ponto não foi antevisto. No momento da sua aprovação para o mercado, a FDA condicionou o uso da terapia à realização de um teste prévio da função pulmonar do paciente. Na ocasião esta restrição não foi considerada um problema, porque os clínicos gerais já estavam acostumados e treinados a utilizar o equipamento deste teste (espirômetros) para seus pacientes com asma/bronquite. Porém, a estratégia inicial da Pfizer era iniciar a adoção da droga pelos endocrinologistas já treinados em longos ciclos de capacitação pela empresa para manipular o dispositivo inalador do Exubera (Adner, 2012).
Os endocrinologistas não possuíam tais equipamentos em seus consultórios (não era necessário) e a disposição do médico em atrasar o tratamento marcando uma consulta prévia em um clinico geral não foi suficiente (bem como a disposição do paciente em esperar o retorno ao endocrinologista – normalmente demorado pela escassez deste profissional no mercado norte-americano). A Pfizer subestimou o momento de translação T3 da disposição à adoção na prática médica, e acabou arcando com um custo total de US$ 2,8 bilhões. O fracasso impossibilitou uma mudança fundamental na qualidade de vida de milhões de pessoas com Diabetes.
Percebe-se a criticidade de se considerar os riscos de adoção, que ultrapassam a própria organização e começam a chamar a atenção da importância dos outros agentes na cadeia (regulatório, comunidade médica, paciente, investidores/planos de saúde, gestores públicos) corresponsáveis pela difusão e aceitação do novo produto. Khoury et al. (2007) e Brownson et al. (2012) destacam a ainda negligência com esta fase translacional, e a emergência de um novo ramo da PT voltado à pesquisa de implementação (que estuda as formas de intervenção necessárias para implementar uma nova terapia/produto), e de difusão (as influências das redes de agentes colaterais na maneira pela qual o sistema social e de saúde recebe a inovação).
Esta fase translacional avalia os impactos na saúde a partir da adoção das terapias ou medicamentos, uma vez implementados os protocolos ou guidelines baseados em evidências. Khoury et al. (2007) destacam a importância do acompanhamento dos resultados para o estabelecimento de novas estratégias de adoção (em T3, por exemplo), na identificação de mudanças necessárias nos protocolos clínicos (T2) ou mesmo na descoberta de outras possíveis aplicações clínicas (em T1) (Wehling, 2010).
É possível, portanto, considerar parte do escopo desta etapa os estudos de farmacovigilância, por exemplo, e a implementação de eventuais políticas públicas baseadas nas evidências da prática e consumo. Neste ponto, Wethington; Dunifon (2012) ressaltam a importância do acesso às diversas associações de grupos engajados nos direitos de pacientes de determinada doença (organizações profissionais, grupos de advogados etc.), e que possuem muitas vezes informações valiosas, pois monitoram o comportamento tanto dos médicos quanto dos pacientes através de pesquisas e surveys. Estas e outras formas de trazer o paciente para o debate do consumo, são essenciais nesta fase da translação para conjugar as informações que os pesquisadores (básicos e clínicos) necessitam com as demandas dos usuários/pacientes.
Este movimento de utilização das evidências produzidas na prática chama-se Evidence-Based Practice (EBP) e deriva do movimento da Medicina Baseada em Evidências (MBE), expandido para a utilização de um conjunto maior de evidências que não somente aquelas de origem médica, centrando o paciente como agente, e trazendo a importância de se estudar outras questões que influenciam o sucesso do tratamento – sociais, culturais, comportamentais, etc. (Palinkas; Soydan, 2012, Wethington; Dunifon, 2012).
A partir do estudo e compreensão dos momentos translacionais, pode-se concluir que a interação entre as fases de translação é dinâmica e não-linear. Isto porque, além de muitas atividades destas fases ocorrerem em paralelo, elas necessariamente precisam de feedbacks constantes. Os gaps translacionais da cadeia coexistem e não há possibilidade de avaliar adequadamente T1 apenas considerando T2, por exemplo. É necessário que T1 esteja alinhado com T2, T3 e T4. A cadeia produtiva objeto da análise translacional, portanto, passa a assumir uma configuração mais flexível aos espaços de conexão e integração entre as suas principais atividades de modo a facilitar a avaliação das fases T presentes na cadeia.
A relevância da pesquisa reside basicamente na aproximação das áreas de conhecimento da Engenharia (em especial a Engenharia de Produção) e da Medicina, em termos de aprendizados recíprocos e seus consequentes avanços na literatura para tratamento de problemas afetos aos dois campos, no que diz respeito a cadeias produtivas de medicamentos, a partir da perspectiva translacional. Esta nasce da motivação de tratar os “gaps” da cadeia produtiva de medicamentos que afligem atores diversos na provisão e acesso mais efetivos de novas terapias e/ou medicamentos.
Silva (2014) observa nas Ciências Biomédicas uma oportunidade de aprendizado para a Engenharia, em especial no campo da Gestão. A Pesquisa Translacional é umas das soluções da chamada Medicina Baseada em Evidências (MBE) ou do inglês, Evidence-Based Medicine (EBM) na realização de pesquisas centradas em evidências da prática, no intuito de aproximar “as ciências das profissões” – problema ainda mal resolvido no campo da Gestão (Silva, 2014).
No entanto, a própria existência da Pesquisa Translacional, como campo do conhecimento, sugere que a Medicina ainda não resolveu completamente este “gap” entre a pesquisa e a prática (Wehling, 2010). A ênfase nesta nova disciplina indica o caminho do entendimento do problema, mas não necessariamente uma “fórmula” de resolução. Neste aspecto há contribuições importantes da Engenharia para o campo (National Institutes of Health, 2006, Zerhouni, 2006, Wadman, 2010).
A Engenharia de Produção pode (e deve) buscar “novas lentes” em outras disciplinas e áreas do conhecimento, a fim de potencializar sua contribuição (neste caso, em especial, no campo da análise de cadeias produtivas ou cadeias de suprimento), particularmente pela sua característica interdisciplinar (Batalha et al., 2007). No caso desta pesquisa, a busca desta nova lente propõe um intercâmbio da área das Engenharias com as das Ciências Biomédicas, em que a Pesquisa Translacional como abordagem interdisciplinar se coloca como elo central.
No que diz respeito ao campo da Gestão da Cadeia de Suprimentos em particular, a relevância teórica da pesquisa se sustenta na possibilidade de incorporar uma nova abordagem de representação e de análise de cadeias produtivas de medicamentos, que contribua para o preenchimento de algumas lacunas existentes no escopo atual da disciplina para este objeto em especial. Este aspecto está intimamente relacionado com a questão central de pesquisa, que pretende verificar, pelo menos em um plano experimental, o alcance desta contribuição. Desta forma, conclui-se que a abordagem translacional foi capaz de ampliar o escopo de estudo da disciplina de Gestão de Cadeias de Suprimentos, incorporando novos agentes de interesse e uma nova maneira de representar a interconexão de suas atividades.
Adner, R. (2012). The wide lens: A new strategy for innovation. Penguin UK.
Alving, B.; Dai, K.; Chan, S. H. H. (2012) Translational Medicine - What, Why and How: An International Perspective. 1 ed. [s.l.] S. Karger
Batalha et al. (Org.) (2007). Introdução à Engenharia de Produção. 1 ed. Rio de Janeiro: Elsevier – Campus.
Baumann, M. et al. (2001). The translational research chain: Is it delivering the goods? International Journal of Radiation Oncology Biology Physics, v. 49, n. 2, p. 345–351.
Baxter, K. et al. (2013) An End to the Myth: There Is No Drug Development Pipeline. Science Translational Medicine, v. 5, n. 171, p. 171.
Bozza, F. A. & Neto, H. C. C. F. (2011) Pesquisa translacional aplicada a medicina intensiva. Revista Med D'Or. Edições de 2011. Número 1. Terapia Intensiva. Disponível em https://goo.gl/VQC9P0. Acessado em setembro de 2013
Brownson, R. C.; Colditz, G. A.; Proctor, E. K. (2012). Dissemination and implementation research in health: translating science to practice. Oxford University Press.
Califf, R. M.; Berglund, L. (2010) Linking scientific discovery and better health for the nation: the first three years of the NIH’s Clinical and Translational Science Awards. Academic medicine: journal of the Association of American Medical Colleges, v. 85, n. 3, p. 457–462.
Chiesa, V., & Chiaroni, D. (2005). Industrial clusters in biotechnology: driving forces, development processes, and management practices. London: Imperial College Press.
Christopher, M. (1998). Logística e gerenciamento da cadeia de suprimento. São Paulo: Thomson.
Coller, B. S.; Califf, R. M. (2009). Traversing the valley of death: a guide to assessing prospects for translational success. Science Translational Medicine, v. 1, n. 10, p. 10.
Collins, F. S. (2011). Reengineering Translational Science: The Time Is Right. Science Translational Medicine, v. 3, n. 90.
Curry, S. H. (2008). Translational science: Past, present, and future. Biotechniques, 44.
Fitzgerald, G. (2010a). Drug development needs a new brand of science. Nature, v. 468, n. 7326, p. 869.
Fitzgerald, G. (2010b). Perestroika in Pharma: Evolution or Revolution in Drug Development? Mount Sinai Journal of Medicine, v. 77, n. 4, p. 327–332.
Ford, D., Gadde, L., Hakansson, H. et al. (2003) Managing Business Relantionships. 2 ed. John Wiley & Sons.
Guimaraes, R. (2013). Translational research: an interpretation. Ciencia & Saude Coletiva, v. 18, n. 6, p. 1731–1744.
Jaberidoost, M. et al. (2013). Pharmaceutical supply chain risks: a systematic review. Daru-Journal of Pharmaceutical Sciences, v. 21, p. 69.
Kazemzadeh, R. B.; Sepehri, M. M.; Jahantigh, F. F. (2012) Design and Analysis of a Health Care Supply Chain Management. In: Zhang, C. S. (Ed.). Materials Science and Information Technology, Pts 1-8. [s.l: s.n.]. v. 433-440p. 2128–2134.
Khoury, M. J., Gwinn, M., Yoon, P. W., Dowling, N., Moore, C. A., & Bradley, L. (2007). The continuum of translation research in genomic medicine: how can we accelerate the appropriate integration of human genome discoveries into health care and disease prevention?.Genetics in Medicine, 9(10), 665-674.
Lambert, D. M. [et al] (1998) Administração estratégica da logística. São Paulo: Vantine Consultoria.
National Institutes Of Health (2006) NIH Roadmap for Medical Research, Fact Sheet.
Nordstrom, R. J. Models for translational research in biomedicine - art. no. 64301V. In: Vodinh, T. et al. (2007). Advanced Biomedical and Clinical Diagnostic Systems V. Bellingham: Spie-Int Soc Optical Engineering.
Palinkas, L. A.; Soydan, H. (2012). Translation and implementation of evidence-based practice. New York: Oxford University Press.
Porter, M. E. (1985). Competitive advantage: creating and sustaining competitive performance. New York: Free Press.
PubMed (2012). Disponível em: https://goo.gl/5bftw6. Acesso em: jun.2014.
Rees, H. (2011). Supply Chain Management in the Drug Industry: Delivering Patient Value for Pharmaceuticals and Biologics. 1 ed. [s.l.] Wiley.
Sackett, D. L. et al. (1996). Evidence based medicine: what it is and what it isn’t. BMJ (Clinical research ed.), v. 312, n. 7023, p. 71–72, 13 jan. 1996.
Silva, E., Proença Jr., D. (2013.) Revisão Sistemática da Literatura em Engenharia de Produção. Rio de Janeiro: Édison Renato Pereira da Silva.
Silva, É. R. P. (2014). Duality in a volcanic temple: a critical assessment of management’s never-ending crisis (Doctoral dissertation, Universidade Federal do Rio de Janeiro).
Slack, N., Chambers, S., & Johnston, R. (2010). Operations Management (6th ed.). Pearson - Financial Times Prentice Hall.
Straus, S. E., Glasziou, P., Richardson, W. S. & Haynes, R. B. (2011). Evidence- based medicine: How to practice and teach it. Edinburgh: Elsevier/Churchill Livingstone.
Trochim, W. et al. (2011). Evaluating translational research: a process marker model. Clinical and translational science, v.4, n. 3, p. 153–162.
Wadman, M. (2010). NIH encourages translational collaboration with industry. Nature reviews. Drug discovery, v. 9, n. 4, p. 255–256.
Wehling, M. (2006). Translational medicine: can it really facilitate the transition of research “from bench to bedside”? European Journal of Clinical Pharmacology, v. 62, n. 2, p. 91–95.
Wehling, M. (2010). Principles of translational science in medicine: from bench to bedside. Cambridge; New York: Cambridge University Press.
Wethington, E.; Dunifon, R. E. (2012). Research for the public good: applying the methods of translational research to improve human health and well-being. Washington, DC: American Psychological Association.
Woods, N. F.; Magyary, D. L. (2010). Translational research: why nursing’s interdisciplinary collaboration is essential. Research and theory for nursing practice, v. 24, n. 1, p. 9–24.
Zerhouni, E. A. (2006). Clinical research at a crossroads: The NIH roadmap. Journal of Investigative Medicine, v. 54, n. 4, p. 171–173.
1. Mestre em Engenharia de Produção, Bio-Manguinhos/Fiocruz, lethiciavivas@gmail.com
2. Mestre em Engenharia de Produção, professora substituta da Universidade Federal do Rio de Janeiro, mariaclara.lippi@ufrj.br
3. Doutor em Engenharia de Produção, professor da Universidade Federal Fluminense, guidovazsilva.gpi@gmail.com
4. Doutor em Engenharia de Produção, professor da Universidade Federal Fluminense, lllnavarro@gmail.com
5. Doutor em Engenharia de Produção, professor da Universidade Federal do Rio de Janeiro, adriano@gpi.ufrj.br